- Современные алгоритмы антидепрессивной терапии предполагают длительные курсы лечения, поэтому переносимость антидепрессанта с минимизацией поведенческой токсичности необходима для обеспечения полноценного социального функционирования пациентов. В частности, антидепрессанты с выраженным седативным компонентом действия могут замедлять время реакции и ухудшать внимание, негативно влияя на способность к управлению транспортным средством. В статье приводятся современные данные о подходах к антидепрессивной терапии у водителей, в том числе о дополнительных факторах, повышающих риск аварий на фоне приема антидепрессантов. Обосновываются критерии выбора антидепрессанта для минимизации рисков, связанных с вождением.
По данным метаанализов, современные АД обнаруживают определенные различия по структуре побочных эффектов, что необходимо учитывать в индивидуальных назначениях, особенно если имеются сведения о нежелательных явлениях, развивавшихся у пациента в процессе тимоаналептической терапии ранее [1, 2]. Например, среди селективных ингибиторов обратного захвата серотонина (СИОЗС) флуоксетин считается лидером по частоте гастроинтестинальных расстройств, флувоксамин – по частоте тошноты, пароксетин – потливости и седации, сертралин – диареи. При этом частота тошноты и рвоты при приеме дулоксетина и венлафаксина (СИОЗС и норадреналина – СИОЗСН) выше, чем у препаратов группы СИОЗС. При приеме миртазапина и пароксетина отмечается значительная прибавка массы тела, а миртазапина и тразодона – выраженная седация.
Согласно рекомендациям S.Kennedy и соавт. «Canadian Network for Mood and Anxiety Treatments» [3] по фармакологическому ведению пациентов с большим депрессивным расстройством, прием АД должен длиться 6–9 мес после достижения симптоматической ремиссии, а при повышенном риске рецидива – 2 года и более. Имеются данные, подтверждающие это положение [см. 4-6]. При резком прекращении приема АД до 40% пациентов могут испытывать симптомы отмены (бессонница, тошнота, потеря равновесия, сенсорные расстройства, повышенная возбудимость и др.) [7].
Приоритетными при выборе препарата становятся минимальная выраженность поведенческой токсичности и спектр побочных действий. Особое значение в этом случае приобретают индивидуальная чувствительность и исходное отношение больного к антидепрессанту и психофармакотерапии в целом. В качестве препаратов выбора выступают АД различной структуры, сочетающие мягкий тимоаналептический эффект с хорошей переносимостью [9].
Хорошая переносимость АД терапии с минимизацией явлений поведенческой токсичности актуальна для обеспечения активного социального функционирования пациентов, что в современном обществе часто связано с необходимостью вождения автомобиля. АД с выраженным седативным компонентом действия могут замедлять время реакции и ухудшать внимание, тем самым негативно влияя на способность к управлению транспортным средством.
Метаанализ от 2017 г., включивший данные исследований 1995–2015 гг., показал 40% повышение риска аварии и более чем трехкратное повышение риска попасть в аварию со смертельным исходом у водителей, принимавших АД [11]. Доступные зарубежные обзоры выделяют и дополнительные факторы, повышающие риск аварий на фоне терапии АД.
Трициклические антидепрессанты (ТЦА), к которым относятся амитриптилин, имипрамин, а также активные метаболиты нортриптилин, дезипрамин и доксепин, повышают вероятность аварии в среднем на 41% [12]. Механизмы, определяющие этот риск, связаны не только с седацией, в разной степени характерной для всех ТЦА, но и с антихолинергическим действием, влияющим на зрение, и риском ортостатической гипотензии.
K.Iwamoto и соавт. выявили прямую корреляцию между уровнем амитриптилина в плазме и способностью совершения маневров (через 4 ч после приема 25 мг) [13].
A.Brunnauer и соавт. показали, что только 10% пациентов, получающих ТЦА, способны сдать тест на вождение (Global Driving Ability Test), в то время как среди пациентов, принимающих миртазапин, эта цифра выше, хотя и не превышает 50% [14].
В норвежском исследовании J.Bramness и соавт. сравнили 2 группы пациентов: получавших седативные (ТЦА и миртазапин) и неседативные АД. Установлено, что в 1-й группе риск ДТП был на 40% выше [15].
Пожилой возраст и использование более высоких доз значимо увеличивают риск аварии на фоне терапии амитриптилином. Применение 125 мг амитриптилина у пожилых повышает риск аварии на 220–230%[16-17].
Фактически даже использование субтерапевтических доз ТЦА, недостаточных для адекватной терапии депрессии, ухудшает психомоторные функции и визуальное восприятие, что позволяет отнести ТЦА к последней линии терапии депрессии у водителей при наличии альтернативы [14].
СИОЗС и другие современные АД продемонстрировали преимущество по сравнению с ТЦА в отношении влияния на избирательность внимания [14], и, казалось бы, проблема выбора должна быть решена. Однако в обзорах, посвященных влиянию современных АД на способность к вождению, было отмечено, что данные носят «неясный и противоречивый» характер. Возможно, это обусловлено неоднородностью группы препаратов, включенных в исследования. Так, M.Wingen и соавт. сообщили об ухудшении маневрирования транспортным средством в тесте SDLP (Standard Deviation Lateral Position) при использовании как СИОЗС, так и СИОЗСН, но не рассматривая каждый препарат в отдельности [18].
Серьезные различия имеются между плацебо-контролируемыми исследованиями, проведенными в «стерильных» условиях научного эксперимента, и наблюдательными исследованиями из реальной жизни. Например, двойное слепое плацебо-контролируемое исследование 1998 г. показало отсутствие влияния венлафаксина на тест SDLP [19], а данные натуралистических наблюдений A.LeRoy и cоавт. зафиксировали увеличение риска аварий на фоне приема венлафаксина (78%). Аналогичные данные были получены для дулоксетина (78%) и еще в большей степени – для тразодона и нефазадона (90%) [12]. Подобные риски были обнаружены и в объемном наблюдательном исследовании J.Bramness и соавт. [15].
Для понимания значимости риска аварии, связанного с АД терапией, некоторые авторы приводят эквивалентные риски, связанные с уровнем алкоголя в крови, среди них результаты 5-летнего когортного наблюдения за 409 171 взрослым жителем штата Вашингтон. Различные седативные препараты, в том числе и антидепрессант тразодон, принимали 5,8% пациентов (табл. 1) [20].
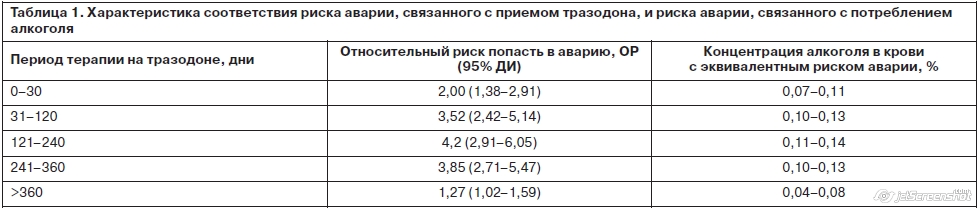
Пик риска аварий отмечен на 4–8-м месяце терапии, что вступает в противоречие с мнением о возможности полной адаптации к АД спустя 1–2 недели терапии [21] и с мнением, что риск связан исключительно с симптомами депрессии, которая сама по себе может влиять на скорость психомоторных реакций и почти удваивает вероятность ДТП [11].
В целом к факторам, доказано повышающим риск аварий у водителей, принимающих АД, относятся:
- пожилой возраст;
- 1-я неделя терапии;
- резкое повышение дозировки;
- более высокая степень тяжести депрессии;
- взаимодействие по системе цитохрома при одновременном применении других препаратов, обладающих угнетающим действием на ЦНС
[22].
Подтверждение негативного влияния комбинированной терапии современными АД с другим препаратами на способность к управлению автомобилем было получено в исследовании C.Des las Cuevas и соавт. При сочетании СИОЗС или СИОЗСН и других препаратов, влияющих на ЦНС, подавляющее большинство пациентов (80%) не смогли пройти электронные тесты, необходимые для получения водительских прав в Испании [23].
Повышать риски, связанные с вождением автомобиля, могут следующие группы психотропных препаратов [21]:
- Барбитураты – повышают риски в 7,5 раза.
- Бензодиазепины (БЗД) удваивают риск аварий.
- Антипсихотики II поколения повышают риски на 120%.
- Небензодиазепиновые гипнотики: суммарно золпидем, залеплон, эсзопиклон повышали риск на 48%. Причем в группе, принимавшей золпидем, риск увеличивался более чем в два раза по сравнению с контрольной группой
[20]. - Антипаркинсонические средства вызывают внезапные «сонные атаки» почти у каждого третьего пациента
[23].
Риски сочетания АД и указанных групп могут заключаться не только в наложении седативных эффектов, но и в значительном повышении концентрации веществ при совпадении в пути выведения по ферменту в системе цитохрома. Многие АД из групп СИОЗС и СИОЗСН являются мощными ингибиторами системы цитохрома P450 и могут значительно повышать концентрацию препаратов из группы риска для водителей (табл. 2). Например, флуоксетин и флувоксамин замедляют выведение триазоловых БЗД (триазолам, алпрозалам, мидозалам), т.е. повышая их концентрацию и, соответственно, выраженность побочных эффектов (ухудшение внимания и реакции, седация, головокружение и др.) [11].
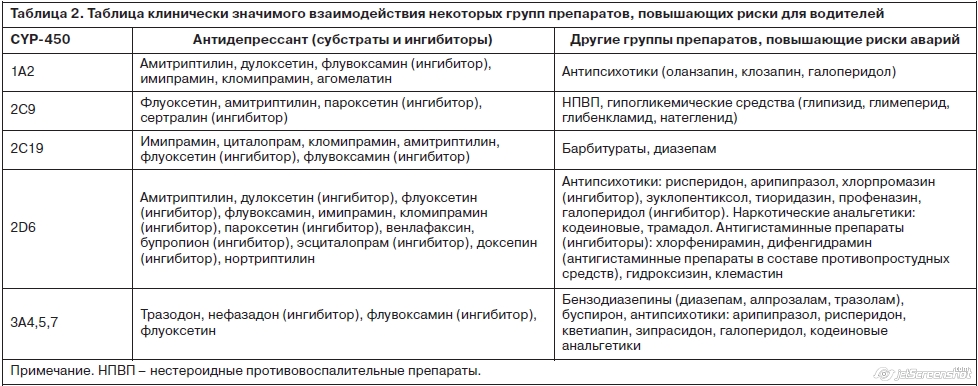
АД могут повышать концентрацию препаратов соматической терапии, увеличивающих риски для водителей: для мышечных миорелаксантов – +209%, для инсулина – в 1,8 раза, для метформина и препаратов сульфонил мочевины – в 1,5 раза (риски, связанные с развитием гипогликемических состояний). Выявлены риски у седативных антигистаминных препаратов (в том числе комплексные противопростудные средства), антиспастических, гастроинтестинальных и противорвотных средств с антихолинергическим (атропиноподобным) действием (см. табл. 2) [24].
Следует отметить, что субстраты конкурируют за выведение через фермент и возрастают уровни обоих препаратов, тогда как ингибиторы повышают концентрации других препаратов, выводящихся этим ферментом. Например, комбинация флувоксамина и агомелатина (нерекомендованная) может увеличивать концентрацию агомелатина в 12–412 раз в зависимости от врожденной активности ферментной системы CYP1A2 [25].
АД из всех групп способны потенцировать действие алкоголя, что может проявляться в передозировке, сонливости или головокружении [11].
Исходя из представленных данных хорошей альтернативой для лечения депрессии у лиц, управляющих автомобилем, может стать милнаципран (Иксел). Иксел не взаимодействует с мускариновыми, гистаминовыми и a1-адренорецепторами, селективно действуя только на серотониновые и норадреналиновые транспортеры. В своем классе (СИОЗСН) в терапевтической дозе препарат обладает наиболее норадренергическим действием. Как известно, именно дефицит норадреналина при депрессии снижает способность к концентрации внимания.
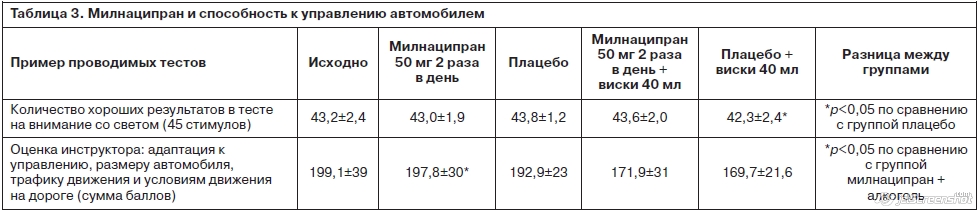
В плацебо-контролируемом исследовании было продемонстрировано, что милнаципран достоверно (p<0,05) улучшал внимание у пожилых пациентов[27]. В двойном слепом плацебо-контролируемом перекрестном исследовании, как в лабораторных тестах, так и в реальной дорожной ситуации, милнаципран (50 мг 2 раза в день) достоверно не ухудшал способности к вождению. Препарат не потенцировал, а в некоторых тестах ослаблял действие низких доз алкоголя (табл. 3) [28].
Милнаципран выделяется среди других АД отсутствием взаимодействия с системой цитохрома. Согласно инструкции «даже в концентрациях, в 25 раз превышающих среднетерапевтические, не влияет на систему микросомального окисления в гепатоцитах.., в силу чего не следует ожидать взаимодействия с индукторами и ингибиторами микросомального окисления».
К критериям выбора антидепрессанта для водителей можно отнести следующие параметры:
- АД не должен вызывать седацию или миорелаксацию, обладать холинергическим или антигистаминным действием, угнетать ЦНС (в том числе у пожилых пациентов), желательно избежать потенцирование действия алкоголя;
- АД должен иметь понятный механизм улучшения когнитивных функций, в первую очередь способности к активации психомоторных реакций и внимания, сниженных в результате депрессии;
- АД должен обладать низким потенциалом лекарственных интеракций, в идеале – характеризоваться отсутствием метаболизма в системе цитохрома, поскольку невозможно исключить необходимость комбинированной терапии в процессе длительного лечения депрессий.
1. Brambilla P, Cipriani A, Hotopf M, Barbui C. Side-effect profile of fluoxetine in comparison with other SSRIs, tricyclic and newer antidepressants: a meta-analysis of clinical trial data. Pharmacopsychiatry 2005; 38 (2): 69–77. 2. Gartlehner G, Hansen RA, Morgan LC et al. Second-generation antidepressants in the pharmacologic treatment of adult depression: an update of the 2007 comparative effectiveness review. Rockville (MD). Agency for Healthcare Research and Quality (US) 2011; 12-EHC012-EF. 3. CANMAT 2016 Clinical Guidelines for the Management of Adults with Major Depressive Disorder: Section 3. Pharmacological Treatments. Can J Psychiat 2016; 61 (9): 540–60. 4. Sim K, Lau WK, Sim J et al. Prevention of relapse and recurrence in adults with major depressive disorder: systematic review and meta-analyses of controlled trials. Int J Neuropsychopharmacol 2015; 19 (2): pyv076. 5. Borges S, Chen YF, Laughren TP et al. Review of maintenance trials for major depressive disorder: a 25-year perspective from the US Food and Drug Administration. J Clin Psychiatry 2014; 75: 205–14. 6. Trivedi MH, Dunner DL, Kornstein SG et al. Psychosocial outcomes in patients with recurrent major depressive disorder during 2 years of maintenance treatment with venlafaxine extended release. J Affect Disord 2010; 126: 420–9. 7. Fava GA, Gatti A, Belaise C et al. Withdrawal symptoms after selective serotonin reuptake inhibitor discontinuation: a systematic review. Psychother Psychosom 2015; 84: 72–81. 8. Renoir T. Selective serotonin reuptake inhibitor antidepressant treatment discontinuation syndrome: a review of the clinical evidence and the possible mechanisms involved. Front Pharmacol 2013; 4: 45. 9. Романов Д.В. Алгоритмы дифференцированной терапии депрессий с применением современных антидепрессантов. Психиатрия и психофармакотерапия. 2012; 14 (2): 56–60. 10. IMS http://www.ims-retail.ru 11. Hill LL, Lauzon VL, Winbrock EL et al. Depression, antidepressants and driving safety. Inj Epidemiol 2017; 4 (1): 10. DOI: 10.1186/s40621-017-0107-x 12. LeRoy AA, Morse ML. Department of Transportation. HS 810 858. Multiple medications and vehicle crashes: analysis of databases. 2008. 13. Iwamoto K, Takahashi M, Nakamura Y et al. The effects of acute treatment with paroxetine, amitriptyline, and placebo on driving performance and cognitive function in healthy Japanese subjects: a double-blind crossover trial. Hum Psychopharmacol Clin Exp 2008; 23: 399–407. 14. Brunnauer A, Laux G, Geiger E et al. Antidepressants and driving ability: results from a clinical study. J Clin Psychiatry 2006; 67: 1776–81. [PubMed: 17196059] 15. Bramness JG, Skurtveit S, Neutel CI et al. Minor increase risk of road traffic accident after prescriptions of antidepressants: a study of population registry data in Norway. J Clin Psychiatry 2008; 69: 1099–103. 16. Ray WA, Fought RL, Decker MD. Psychoactive drugs and the risk of injurious motor vehicle crashes in elderly drivers. Am J Epidemiol 1992; 136: 873–83. [PubMed: 1442753] 17. Leveille SG, Buchner DM, Koepsell TD et al. Psychactive medications and injurious motor vehicle collisions involving older drivers. Epidemiology 1994; 5: 591–8. [PubMed: 7841240] 18. Wingen M, Ramaekers J, Schmitt J. Driving impairment in depressed patients receiving long-termantidepressant treatment. Psychopharmacology 2006; 188: 84–91. [PubMed: 16865389] 19. O'Hanlon JF, Robbe HW, Vermeeren A et al. Venlafaxine's effects onhealthy volunteers' driving, psychomotor, and vigilance performance during 15-day fixed and incremental dosing regimens. J Clin Psychopharmacol 1998; 18: 212–21. [PubMed: 9617980] 20. Hansen R, Boudreau D, Grossman D et al. Sedative Hypnotic Medication Use and the risk of Motor Vehicle Crash. Am J Pub Health 2015; 105 (8). 21. Hetland A, Carr D Ann Pharmacother. Medications and Impaired Driving. Rev Liter 2014; 48 (4): 494–506. 22. Sansone R, Sansone L. Driving on antidepressants: cruising for a crush? Psychiatry (Edgemont) 2009; 7 (9): 13–6. 23. Des las Cuevas C, Sanz EJ. Fitness to drive of psychiatric patients. Prim Care Companion 2008; 10: 384–90. 24. Indiana University Department of Medicine Clinical Pharmacology P450 Drug Interactions "Clinically Relevant". 25. SnPc agomelatine, EMA 2008. 26. Nutt DJ Relationship of neurotransmitter to the symptoms of major depressive disorder. J Clin Psychiatry 2008; 69 (Suppl. E1): 4–7. 27. Hindmarch I, Rigney U, Stanley N, Briley M. Pharmacodynamics of milnacipran in young and elderly volunteers. Br J Clin Pharmacol 2000; 49 (2): 118–25. 28. Richet F, Marais J, Serre C, Panconi E. Effects of milnacipran on driving vigilance Int J Psychiatry Clin Pract 2004; 8 (2): 109–15.
Источник: Петрова Н.Н., Маркин А.В. Антидепрессивная терапия и социальное функционирование: выбор антидепрессанта для водителей. Психиатрия и психофармакотерапия. 2018; 20 (1): 27–31.

